김민정 DS증권 연구원은 "차세대 알츠하이머병 치료제 개발 타깃은 ApoE4 유전자조절과 신경염증(neuro-inflammation) 유발 TREM2"라고 말했다.
김 연구원은 24일 한국바이오의약품협회(KoBIA)가 주관한 알츠하이머 치료제 개발동향과 시장전략 웨비나에서 '알츠하이머 치료제 - 미충족 수요를 향한 다각적 시도'란 주제로 발표했다.
그는 차세대 타깃으로 알츠하이머병(AD)의 가장 강력한 리스크 원인으로 알려진 ApoE4를 꼽았다.
ApoE는 299개의 아미노산으로 구성된 지질 운반 단백질이다. 중추신경계(CNS)에서 주요 운반체로 기능하는 필수적인 단백질이다.
ApoE4는 3개의 대립유전자로 이뤄진다. ApoE2는 AD 보호효과를, ApoE3는 평균적인 효과를, ApoE4는 AD를 유발 가능성을 높이는 것으로 알려졌다.
이런 ApoE 유전자는 단 2개의 단일염기 변화로 인한 차이다. 때문에 일반적으로 사용하는 RNAi, ASO 등의 유전자 발현을 넉다운(knock-down)시키는 접근법으로는 한계가 있다. 정확히 원하는 유전자만 조절하기 어렵기 때문이다.
김 연구원은 "국내에서는 알지노믹스가 ApoE4를 ApoE2로 전환하는 기전의 약물을 개발 중"이라며 "여러 돌연변이를 한번에 교정하는 멀티 교정 방식으로 전체 RNA에는 제한이 없다"고 설명했다.
그는 "현재 해당 약물은 in vivo에서 28일차 생체내 유전자 전달을 확인한 상태로 전임상 연구를 진행중"이라며 "오는 2028년 임상시험계획(IND)을 제출하는 것을 목표로 하고 있으며, 올해부터 라이선스아웃(L/O)를 추진한다"고 덧붙였다.
김 연구원은 "ApoE4를 타깃하는 약물은 렉세오 테라퓨틱스(Lexeo Therapeutics)의 데이터를 볼때 가능성이 있다고 판단된다"고 분석했다.
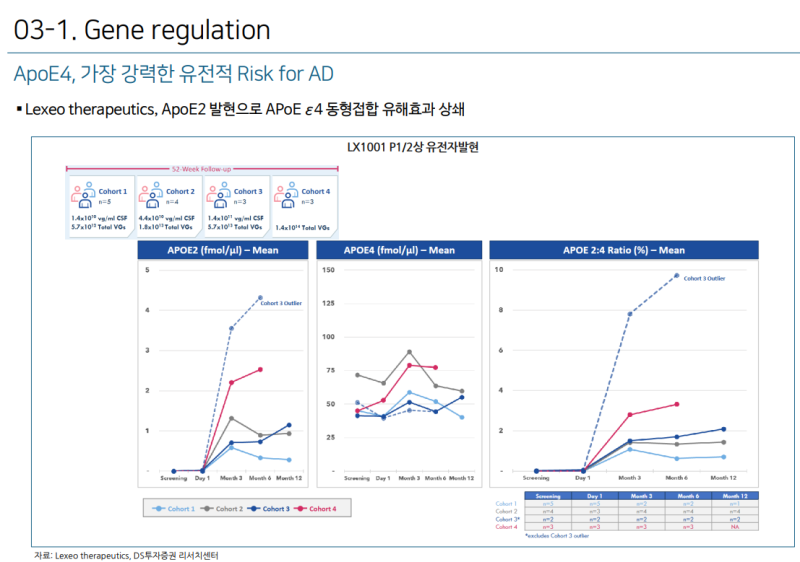
렉세오는 ApoE4 동형접합(homozygote)로 인한 유해효과를 상쇄하는 컨셉의 신약 후보물질 'LX1001'을 개발했다. ApoE4 동형접합체를 가진 CNS에서 ApoE4를 발현해 ApoE2/4 이형접합체(heterozygote) 유사상태로 전환시켜 알츠하이머병 발병위험을 낮추는 컨셉이다.
렉세오는 총 15명을 대상으로 임상1/2상을 진행했으며, 지난 2024년 10월 결과발표 이후 해당 에셋의 연구는 중단했다. 현재는 심장질환에 대한 유전자치료제 기업으로 포지셔닝하고 있다.
김 연구원은 "렉세오의 데이터에서 가능성을 엿볼 수 있었다"며 "ApoE2 고발현 환자에서 타우PET의 감소 효능이 나타나는 경향을 확인했기 때문"이라고 전했다.
그는 "특히 일부 ApoE2 발현이 과하게 나타난 아웃라이어 환자에게서는 PET에서 타우 레벨이 더 효과적으로 감소하는 것이 확인됐다"며 "ApoE2/4 전환이 타우 축적에 효과가 있을 것이란 것을 의미한다. ApoE2 발현을 이전보다 잘 조절하면 ApoE4 동형접합의 유해효과를 상쇄할 수 있는 가능성이 있다는 것으로 여겨진다"고 강조했다.
김 연구원은 미세아교세포(microglia)로 인한 신경염증도 차세대 타깃으로 주목해야 한다고 제시했다.
알츠하이머병은 아밀로이드 단백질 제거이후에도 질병이 계속 진행된다. 따라서 건강한 뇌기능 유지를 위해 신경염증을 저해하는 기전에 관심을 가져야 한다는 것이다.
미세아교세포는 아밀로이드 플라크(plaque) 형성, 시냅스 제거, 타우 단백질 확산(spreading) 등 알츠하이머병 전반에 관여하는 신경면역세포다. 현재까지 이와 관련된 치료제로는 TREM2 작용제(agonist), 보체 억제제, NLRP3 등 이머징 타깃 등이 연구돼 왔다.
TREM2는 미세아교세포의 활성을 조절하는 핵심 조절인자다. 기능을 하지 못하는 변이가 있으면 알츠하이머병 발병위험이 증가하는 것으로 알려졌다.
보체는 미세아교세포 보체 활성화에 의한 시냅스 포식이 퇴행성뇌질환의 발병기전이라는 가설을 기반으로 한다. 실제로 알츠하이머병 모델동물에서 보체 신호경로를 차단할 경우에는 시냅스 기능과 인지장애 기능이 개선된 결과가 확인됐다.
김 연구원은 "TREM2가 주요타깃으로 여겨진다"며 "현재 시장에서는 사노피(Sanofi)가 가장 선두주자"라고 분석했다.
지난 2024년 애브비/알렉토(Abbvie/Alector)는 TREM2 작용제 후보물질 'AL002'의 임상2상에서 실패소식을 알렸다. 당시 가장 앞선 약물로 알츠하이머병 분야에서의 TREM2는 실패한 타깃으로 읽혀졌다.
그러나 지난해 5월 사노피가 TREM2 작용제를 개발하는 비질 뉴로사이언스(Vigil Neuroscience)를 4억7000만달러에 인수하면서 희망의 불씨를 남겼다.
김민정 연구원은 "신경질환 분야에서 4억7000만달러는 큰 베팅은 아니라는 점은 염두에 둬야 한다"며 "그럼에도 TREM2 타깃의 실패로 간주하는 것은 아직 무리가 있다는 판단"이라고 진단했다.
그는 "CNS 침투 제한으로 효능이 충분하지 않았을 가능성과 질병 초기 단계에서 베네핏이 높고, 후기단계에서 효과가 낮았을 가느성 등으로 임상에 적절치 못한 환자군이 채택됐을 가능성 등이 제기된다"고 분석했다.
현재 사노피는 TREM2 작용제 후보물질 SAR448851(VG-3927)의 임상1상은 마무리했다. 다만 아직까지 임상2상 돌입과 관련된 내용은 알려진 바 없다.